بيماري طاعون گاوي (A040 - Rinderpest (RP
Rinderpest
cattle plague
steppe murrain
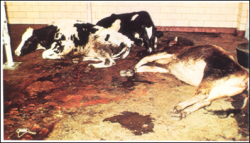
تعریف:
طاعون گاوی یا وبای جلگه ای، یک بیماری عفونی حاد بشدت مسری ومعمولاً کشنده درگاو، گاومیش ، خوک و برخی از گونه های وحش با عامل ویروسی است . بیماری با تب بالا ، تخریش های دهانی ، اسهال ، نکروز لنفاوی و تلافات بالا مشخص می گردد . واژه Rinderpest که آلمانی است به معنی طاعون گاوی است. بیماری موجب درگیری سامانه های روده ای معدی(گوارشی) و تنفسی می گردد.
تاریخچه بیماری:

در اویل قرن هیجدهم بیماری به جهت داشت ضایعات شبه آبله ای ظاهراً مشابه بااین بیماری به نظر می رسید . در طول تاریخ بروز این بیماری غالباً همراه با جنگ ها و عملیات نظامی بوده . قرن هجدهم دوره ای در تاریخچه بیماری است که سه مرحله همه گیری جهانی بیماری (1709-1720 ؛ 1742-1760 ؛ 1768-1786) بوقوع پیوسته و در این بین بویژه اروپا به شدت تحت تهاجم بیماری قرار گرفته . بریتانیا در سال 68/ 1865 با یک همه گیری عمده درگیر بوده . بعدها در سال 1890 بروز یک همه گیری در آفریقای جنوبی و همچنین شاخ آفریقا منجر به تلفات 80 تا 90 درصدی درگاوهای این منطقه جهانی شد . اولین واکسن موثر و موفق توسط سر آرنولد تیلر تهیه شد که به ممانعت از همه گیری منجر شد . همه گیری های دیگری نیز در آفریقا پدیدار گردید(1982-1984) که در نتیجه تلفات دامی خسارتی در حدود 500میلیون دلار را به همراه داشته . پس از ناپدید شدن بیماری از اروپا در اویل قرن نوزدهم بیماری دوبار در جنگ کریمه با چنان گستردگی آغاز شد که تدارکات گوشت برای ارتش های هم پیمان تماماً از گاو های مبتلای بود .
سبب شناسی:
عامل بیماری ویروس پوشش داری کروی یا تخم مرغی شکل با قطر حداکثر 120 تا 300 نانومتر با ژنوم RNA تک رشته ای و قطبیت منفی[1] غیر منقطع(پیوسته) متعلق به خانواده Paramyxoviridae و جنس Morbillivirus است . این ویروس به لحاظ ایمنی زائی در ارتباط با ویروس دیستمپر سگ سانان ، ویروس سرخجه انسانی ، ویروس طاعون نشخوا گنندگان کوچک و موربیلی ویروس های پستانداران دریائی می باشد . ژنوم ویروس با طول 15882 باز در یک پوشش حاوی لیپید محصور گردیده . این ژنوم برای تولید هشت نوع پروتئین رمز گذاری شده دو نوع که از پروتئین های غیرساختاری بوده به نام های V و C . از شش پروتئین ساختاری یعنی فسفو پروتئین P) ) ، پروتئین بزرگ (L) و نوکلئوپروتئین (N) نوکلئو کپسید ساخته شده و ژنوم RNA ویروس را در بر می گیرد . بخش اعظم نوکلئوکپسید پوشاننده ژنوم ویروسی را نوکلئوپروتئین (N) تشکیل می دهد و این نوع پروتئین نقش اصلی را در روند های رونوشت برداری[2] و همانند سازی[3] ویروس بر عهده دارد ، به مجموعه ژنوم RNA ویروس و نوکلئو پروتئین(N) پوشاننده آن ریبونوکلئوپروتئین (RNP)می گویند . ریبونکلئو پروتئین ویروسی که بطور فعال در حال رونوشت برداری است حاوی دو نوع دیگر پروتئین ساختاری ویروسی , یعنی P و L نیز می باشد که این دو پروتئین با هم RNA پلی مراز ویروسی وابسطه به RNA ویروس [4] (RdRP) را تشکیل می دهند . پروتئین های هم آگلوتینین (H)، پروتئین همجوشی(F) و پروتئین ماتریکس(M) به همراه لپیدهای غشائی یاخته میزبان ، پوشش ویروسی را تشکیل می دهند . توالی جایگیری ژنهای مربوط به هر نوع پروتئین ساختاری بر روی ژنوم ویروسی از انتهای ′3 به سمت ′5 به ترتیب عبارتند از 3′-N-P-M-F-H-L-5′)) .
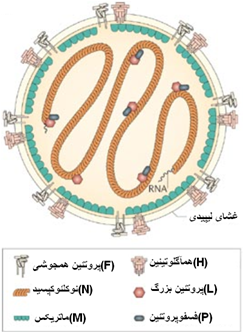

دو نوع پروتئین V,C نیز از ژن P اظهار می شوند. بنا بر این هر ویشه ویروس[5] (ذره کامل ویروس) دارای یک جزء انتقالی و یک جزء نسخه برداری است. جزء انتقالی شامل یک غشای لیپیدی با دو قلاب غشایی خارجی گلیکوپروتئینی به نام پروتئین های هموآگلوتنین (H) و همجوشی (F) است، این پروتئین ها درجهت ورود ویروس به یاخته هدف و رهایش ویروس های تازه تشکیل از یاخته آلوده ایفای نقش می کنند . جزء نسخه برداری(رونوشت برداری) شامل ژنوم RNA ویروسی که با یک نوکلئوپروتئین (N) پوشیده شده و یک مجموعه RNA پلیمراز { تحت واحد بزرگ L) ) و فسفوپروتئین (P)} است . اجزای یاد شده توسط یک پروتئین ماتریکس (M) به یکدیگر متصل شده اند . اعتقاد محققین بر این است که این پروتئین ماتریکس نقش بسیار مهمی را در شکل گیری (تجمیع ساختاری) و بلوغ ذره ویروسی بر عهده دارد . این نقش اساساً از طریق هم آوری دو جزء اصلی ویروس در محل جوانه زنی یاخته میزبان ایفاد می گردد . برای اجرائی شدن این عملکرد ویروسی پروتئین M بایستی بتواند با غشاء یاخته ای میزبان خصوصاً غشای پلاسمائی واکنش نماید. نتیجه واکنش غشای پلاسمائی با خود و همچنین با نوکلئوکپسید مغزی ویروس شکل گیری چند پارها[6] می باشد . همچنین در این واکنش پروتئین M با دنباله سیتوپلاسمی دو پروتئین پوششی ویروس یعنی پروتئین های F وH نیز واکنش خواهد داشت . به محض ورود ویروس به یاخته میزبان (یاخته هدف) روند های همانند سازی و رونوشت برداری توسط پلیمراز ویروسی آغاز می شود . در روند رونوشت برداری ابتداعاً یک RNA رهبر[7] (le-RNA) که متشکل از 52 نوکلئوتید است به همراه شش نوع mRNA تولید می شود . در روند همانند سازی نیز یک RNA قرینه با طول کامل و متعاقباً RNA ژنومی تولید می شود . چرخه حیاطی ویروس با ایجاد پیوند مابین ویروس و یاخته هدف میزبان آغاز می گردد ، برای برقراری این ارتباط ویروسی - یاخته ای گیرنده های خاصی دخالت دارند ، بر روی غشا ی پوششی ویروس پروتئین های هم آگلوتین مسئول ایجاد ارتباط با گیرنده های خاصی در سطح یاخته های میزبانی می باشند ، بعنوان مثال این گیرنده ها در یاخته های لنفوسیتی نوع تیموسی(T) و بورسی (B) و همچنین یاخته های عرضه کننده پادگنی (APC)[8] از نوع CD150 بوده که اصطلاحاً به مولکول فعال ساز لنفوسیت پیام رسان [9](SLAM) نیز معروف هستند . در سطح یاخته های پوششی مخاط گوارشی و دستگاه تنفسی نیز گیرنده هایی وجود دارند که تاکنون ناشناخته مانده اند. پس ازبرقراری این پیوند و با کمک پروتئین همجوشی (F) پوشش ویروس و یاخته مورد تهاجم یکی شده و ژنوم ویروس در داخل سیتوپلاسم یاخته هدف رها می گردد. در داخل سیتوپلاسم یاخته مورد نظر پروتئین کایناز های مختلفی حضور دارند که قادرند بر روی ژنوم ویروسی عمل کنند ، در این میان نوع خاصی از این پروتئین کایناز ها بنام کازئین کایناز نوع دوم[10] در واکنش با فسفوپروتئین ویروس موجب فسفوریله شدن آن شده که از این رو موجب فعال شده مجموعه RNA پلیمرازویروس { تحت واحد بزرگ L) ) و فسفوپروتئین (P)} می شود . نتیجه این فعال سازی آغاز روند های رونوشت برداری و همانند سازی ویروس است . همچنانکه قبلاً نیز عنوان شد در ابتدا شش نوع mRNA و یک le-RNA تولید می شود ، این RNA رهبر باورود به هسته یاخته میزبان موجب توقف روندهای رونوشت برداری ژنوم یاخته میزبانی شده و از طرفی پس از ایجاد پیوند با یک پروتئین هسته ای خاص به نام La مجدداً به سیتوپلاسم یاخته باز می گردد و در آنجا موجب تسریع روند های رونوشت برداری و همانند سازی ژنوم ویروس می گردد .با فراهم شدن ژنوم و پروتئین های ویروسی روند تجمیع ساختاری [11] ویشه ویروسی انجام می شود ، در طی این روند ماتریکس ویروسی(پروتئین M ) پروتئین های غشائی ویروس را که شامل پروتئین همجوشی و هم آگلوتینین است به یکدیگر متصل نموده و از طرفی با حضور آن (ماتریکس) اجزای نسخه برداری و انتقالی ویروس در محل جوانه زنی غشای یاخته میزبانی ، پوشش لیپیدی ویروس را نیز بدست می آورند .
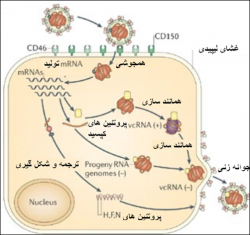
به لحاظ سرم شناسی ویروس تنها دارای یک گروه سرمی است (تنها یک نوع ویروس ایمونوژن دارد) ، ولی از نقطه نظر ژنتیکی دارای اعقابی است که در سه گروه قرار می گیرند ، اعقاب شماره 1 و 2و3 . در گذشته اعقاب فوق در مناطق جغرافیائی متفاوتی دیده می شدند . حدت این ویروس در تغییر بوده و برخی از نژادهای اخیر آن علارغم تلفات شدید در گونه های وحش شکل ملایمی از بیماری را در گاو ایجاد می کنند . نژاد های فوق قابلیت تبدیل به شکل حدت دار در حیوانات اهلی را مجدداً بدست می آورند. نژادهای جدا شده از گاو به لحاظ سرم شناسی و ایمنی شناسی ارتباط نزدیکی باویروس طاعون نشخوارکنندگان کوچک(PPR) دارند.
همه گیرشناسی :
بابروز یک همه گیری در جمعیت حساس دامی میزان شیوع و تلفات بیماری همواره بالا است و درصورت شکست برنامه های کنترلی اولیه و یا عدم امکان غلبه کامل بر همه گیری بایستی دامهای حساس در معرض آلودگی نیز حذف شوند . در مناطقی که بیماری به شکل بومی در آمده ازجهت وجود ایمنی در دامهای منطقه همه گیری های گسترده دیده نشده و مواردی از بروز انفرادی بیماری را می تواند مشاهده کرد . انتشار بیماری از کانون های بومی شده به مناطقی که دارای جمعت دامی حساس هستند میزان ابتلاء تقریباً تا 100درصد گله و میزان تلافات از 25 تا 90 درصد متغییر خواهد بود .
ویروس طاعون گاوی در مقابل تاثیرات محیطی بسیار حساس بوده بطوری که دردمای عادی وخارج از بدن دام تا چند ساعت دوام نداشته و در داخل لاشه طی 24 ساعت در اثر اتولیز و گندیدگی از بین می رود . ویروس تحت اثر حرارت ، خشکی و غالب ترکیبات ضد عفونی کننده (فنل ، کروزول و هیدرواکسید سدیم) به سادگی تخریب می گردد . مقادیر اندک ویروس در دمای 56 درجه سانتی گراد تا 60 دقیقه و دردمای 60 درجه سانتی گراد تا 30 دقیقه پایداری دارد. در مقابل ویروس نسبت به سرما مقاوم بوده وقادر است در خون منجمد شده تا ماه ها فعال بماند. ویروس در PH مابین 4 و 10 پایدار است و مناسب ترین PH برای فعالیت بین 5/6 تا 7 بوده و در PH 2 و 12به سرعت در طی 10 دقیقه غیرفعال می گردد. و به جهت داشتن پوشش لیپیدی به مواد حلال چربی حساس می باشد . ویروس در گوشت آلوده ای که در دمای یخچالی (4درجه سانتی گراد) نگهداری می شود تا یک هفته زنده می ماند . همچنین ویروس در اشیاء و وسائل موجود در جایگاه دام تا چند روز دوام می آورد، به دلیل این عمر کوتاه ویروس در اشیای و محیط خارج ، انتقال بیماری از طریق لباس و اشیای آلوده غیر محتمل است . ویروس در چراگاه بدون سایه تا 6 ساعت و در چراگاه سایه دار18 تا 48 ساعت زنده می ماند. حصارهای محوطه دامداری آلودگی خود را در طی 48 ساعت و ساختمان های آلوده در طی 96 ساعت ازدست می دهند .
تمامی حیوانات سم شکافته[12] به ویروس فوق حساس بوده و دچار عفونت می شوند . گاو، گاومیش ، بوفالوی آبی ، گاومیش افریقائی،گاو کوهی آفریقائی، کودو[13]،بوش پیگ[14]،وارتوق[15]، زرافه، بز های کوهی به ویژه به بیماری حساس هستند . گاووحشی[16] و زبو های(گاوهای کوهان دار) آفریقای شرقی بطور متوسط حساس بوده و غزال ، گوسفند و بز بطور خفیف حساس می باشند . بیماری بندرت در خانواده شتر سانان دیده می شود ولی در صورت تماس نزدیک با گاو احتمال ابتلا وجود دارد. عفونت طبیعی در اثر این ویروس را تنها در گاو و گاومیش می توان دید ولی در برخی از همه گیری ها گوسفندان و بزها نیز مبتلا می شوند و گاهی نیز اولین جمعیت هدف گوسفندان و بزها هستند که بعداً بیماری را به گاو منتقل می کنند . خوکها نیز به ویروس حساس هستند ،به نظر می رسد که خوک های آسیائی در مقایسه با انواع اروپائی و آفریقائی حساس تر باشند. ولی بیماری در آنها تنها با یک تب ملایم تظاهر می نماید ، به هر حال انتشار خوک به خوک ویروس محقق نبوده واصولاً این گونه دامی نقش مهمی را در همه گیری بیمار بر عهده ندارد . نشخوا کنندگان وحشی از عمده منابع اشاعه آلودگی محسوب شده و مانع بزرگی در مقابل ریشه کنی بیماری به شمار می روند . از این حیوانات وحش که عموماً درگیرمی شوند می توان به گونه های آبزی و سایه دوست اشاره نمود . در میان نژادهای گاوی نوع زبو از همه مقاومتر است . شتر های تک گوهانه می توانند دچار عفونت شوند ولی نشانه های بالینی در آنها دیده نمی شود و منبع آلودگی نیز به شمار نمی آیند . نژاد های اوروپائی خوک ها ، گوسفند ، بز ، شترو نشخوا کنندگان وحش ممکن است بعنوان منابع آلودگی برای گاو عمل نمایند . البته باید توجه داشت دام های بهبود یافته از بیماری تنها برای چند روز بعنوان ناقل بیماری عمل می کنند(ناقلین نقاهتی) . چون ویروس طاعون گاوی برای مدت طولانی در محیط زنده نمی ماند حیوانات وحش بعنوان مخازن بیماری عمل نکرده و از این رو کنترل بیماری به سهولت امکان پذیر می گردد. گوزن دم سفید و گرازسفید آمریکایی را بطور تجربی می توان آلوده نمود.
جنس و سن دام بعنوان عامل موثر در ابتلاء به بیماری مطرح نمی باشد. ایمنیت حاصل از آلودگی طبیعی طولانی است ولی در تمامی طول عمر دام باقی نمی ماند . ایمنت حاصل از مایه کوبی تداوم متنوعی دارد و عموماً متناسب با شدت پاسخ بالینی بوجود آمده است . حیوانات بهبود یافته دارای یک ایمنیت سخت بوده و بعنوان یک ناقل مزمن عمل نمی کنند .
ویروس 1تا 2 روز پیش از بروز نشانه های بالینی در ترشحات وجود دارد. ویروس در هوای بازدمی ، ترشحات بینی و چشمی ، بزاق ، خون ، بافت ها، مدفوع ، ادرار، شیر، مایع منی و ترشحات مهبلی حضور داشته ودر اولین هفته بروز نشانه های بالینی یعنی حدوداً در مرحله واکنش افزایش حرارت (تب) به بیشترین میزان خود رسیده و حدوداً یک هفته بعد از برگشت دمای بدن به حد معمول خود که توام است با ظهور پادتن های اختصاصی در سرم به تدریج کاهش می یابد.
تمامی ترشحات دام بیمار حاوی ویروس بوده(عفونی هستند) و دو راه غالب دفع ویروس ترشحات بینی و مدفوع می باشد .تماس نزدیک مابین دام سالم و آلوده برای انتقال و انتشار بیماری امری ضروری به شمار می آید ، این انتقال توسط ترشحات آلوده دام بیمار و عمدتاً ترشحات بینی محقق می شود . البته برسی ها اخیر نشان می دهد که با بالا رفتن رطوبت درشب امکان انتشار بیماری از طریق ذرات آلوده تا مسیر های 100 متری یا بیشتر نیز ممکن می باشد . اعتقاد بر این است که عفونت در نتیجه استنشاق ذرات آلوده و آشامیدن آب آلوده به ویروس حاصل آمده و انتقال بیماری به دیگر مناطق از طریق نقل و انتقال دام های دچار عفونت است ولی دامهای بهبود یافته به جهت ایمنی قوی نقش ناقل مزمن را ایفا نمی کنند . مصرف غذای آلوده به ترشحات دام بیمار یا دامی که در مرحله نهفته بیماری است(ناقل نهفته) یا دامی که دچار عفونت تحت بالینی است ممکن است شیوه مهمی در انتقال عفونت – خصوصاً در خوک – باشد. انتقال عمودی (رحمی) در این بیماری محقق نیست.انتقال بیماری در آفریقا به جهت سیستم نگهداری چادر نشینی و استفاده از نواحی آبی مشترک تسهیل می گردد .
روند بیماری زائی:
با استنشاق ذرات آلوده ویروسی یا بلع گوارشی آب های آلوده ، ویروس وارد بدن دام حساس گردیده و به مخاطات تنفسی وگوارشی می رسد . پس از پیوند با گیرنده های اختصاصی و همجوشی با غشای یاخته های پوششی با آن یکی شده و ژنوم ویروس وارد سیتوپلاسم یاخته می گردد . روندهای مربوط به همانند سازی و رونوشت برداری ویروس چنانکه در بحث سبب شناسی عنوان شد سپری گردیده و نهایتاً ویشه های(ویریون) ویروسی جدیدی پدیدار شده و از یاخته آلوده رها می شوند ، ویروس طاعون گاوی به جهت میل پیوندی به گیرنده های CD150 تمایل زیادی با لنفوسیتها ی موجود در ناحیه مخاطات تنفسی و گوارشی دارد که دارای این نوع گیرنده هستند ، ویروس پس از ورود در یاخته های یاد شده نهایتاً به غدد لنفاوی ناحیه رسیده پس از تکثیر مجدد د ر یاخته های فوق آغاز گر روند های ایمنی زائی بر علیه ویروس خواهد بود که تب یکی از نشانه های آن است . هدف اولیه ویروس در تهاجم به ارگانهای دام حساس بافت های لنفاوی ومخاطات لوله گوارشی است . معمول ترین ضایعات حاصله در بافتهای لنفاوی پیدایش یاخته های غول پیکر[17] و نکروز فولیکول های لنفاوی است . واز طرفی در بافت پوششی مخاطات گوارشی نیز موجب نکروز های کانونی بصورت التهاب دهانی موضعی [18] و التهاب روده ای می گردد که نتیجه مستقیم عفونت ویروسی است . سازو کار های مختلفی را می توان در پیدایش نکروز فولیکول های لنفاوی دخیل دانست : اثر مستقیم کشندگی ویروس بر روی یاخته ها آلوده ؛ اثر تخریبی ویروس بر روی یاخته های مشبک نگهدارنده یاخته های لنفاوی ؛ و دخالت کورتیکواستروئید های آزاد شده در طی روند عفونت . نتیجه چنین ضایعات لنفاوی کاهش شمارش لنفوسیت های خون در طی روند عفونت است . از طرفی ایجاد نکروز در بافتهای لنفاوی همراه لوله گوارشی[19](GLAT) خود سبب بروز اسهال می گردد.
ویروس های جدید از طریق مجاری وابران لنفی به خون رسیده و سبب بروز یک ویرمی می شوند. ویروس در خون بصورت آزاد نبوده و در داخل گویچه های سفید خونی حمل می گردد . یکی از راهکارهای ذاتی مبارزه ای سامانه ایمنی بدن در پستانداران به هنگام مواجه با عوامل ویروسی تولید اینترفرون هایی است که یاخته های آلوده به ویروس را مورد تهاجم قرار می دهند. اینترفرون ها (نوع آلفا و گاما) با واسطه پروتئین های غشائی خاصی به نام پروتئین های فعال کنده رونوشت برداری و مبدل علامتی[20] STATs موجب رونوشت برداری و تولید پروتئین های خاصی در یاخته آلوده می شوند که اثرات ضد ویروسی دارد. معمولاً با بروز ویرمی میزان این اینترفرون ها در سرم تا روز 4 ورود ویروس به خون به اوج خود رسیده ولی پس از آن فروکش می کند . ویروس طاعون گاوی با واسطه پروتئین های P و C و عمدتاً V قادر است که این اثر ضد ویروسی اینتر فرون های نوع آلفا و گاما را مهار نماید . سازوکار این تاثیر مبتنی بر ممانعت از فسفوریلاسیون پروتئین های STAT1 وSTAT2 وجلوگیری ازانتقال آنها به هسته توسط پروتئین های ویروسی در یاخته های آلوده به ویروس است . از طرفی دیگر ویروس طاعون گاوی موجب مهار روند تولید اینترفرون نوع یک(بتا) می شود، اصولاً در یاخته های پستانداران با شروع آلودگی ویروسی پیش ساز اینترفرون نوع بتا فعال می گردد ،پروتئین C ویروس طاعون گاوی موجب مهار این روند فعال سازی می شود . نتیجه این رخدادها ادامه روند تکثیر و گسترش ویروس در بدن دام بیمار است . از روز دوم بروز ویرمی گویچه های سفید خونی دارای ویشه های ویروسی بوده که تا روز 3تا 5 به اوج خود میرسد ، پس از روز هفتم تقریباً تمامی یاخته های حاوی ویشه ویروس حذف می شوند . همزمان با کاهش سطح سرمی اینترفرون ها میزان پادگن های ضد ویروسی در سرم بالا می رود که این رخداد همزمان است با حذف یاخته های خونی حاوی ویروس.
نشانه های بالینی:
دوره نهفته بیماری در موارد میدانی(ابتلاء طبیعی)3تا 15 روز بوده (بطور معمول 4-5 روز) که با وجود مقاومت طبیعی بالا طولانی تر نیز می شود اما در تلقیح تجربی ویروس به دام حساس تنها 2تا3 روز می باشد . اصولاً طول دوره نهفته بیماری تحت تاثیر حدت ویروس ، دوز آلودگی و راه آلودگی می باشد. بیماری در اشکال فوق حاد ، حاد ، تحت حاد ، غیر معمول و شکل پوستی تظاهر می کند . شکل فوق حاد: که اساساً در حیوانات جوان و تازه متولد شده دیده می شود بطور اولیه با بروز یک تب بالا و مرگ ناگهانی مشخص می شود . در شکل حاد(کلاسیک) : بیماری در مرحله نخست که تا چند روزی به طول می انجامد تنها با تب بالای 5/40-5/41 درجه سانتی گراد افسردگی، بی قراری ، تنفس سطحی و سریع و نبض تند بدون هر گونه نشانه موضعی تظاهر می نماید . همراه با بروز تب بی اشتهائی ، کاهش تولید شیر، تراوش اشک دردامی که دارای پوشش سخت وزمخت و درخشان است مشاهده می گردد. پوزه دام خشک بوده و مخاطات قابل روئیت پر خون می باشند . بدنبال این نشانه ها التهاب مخاطات دهانی و بینی و ملتحمه پدیدار شده و ممکن است که مخاطات مهبلی پرخون شده و تورمی در فرج بوجود آید. ترشحات اشکی بیشتر شده و سپس بصورت چرکی درآمده و همراه آن انقباض پلکی ایجاد می گردد . با گسترش ضایعات دهانی ترشحات بزاقی کف آلود (حباب دار) با رنگ خونی روشن ظاهر شده که متعاقباً بصورت بزاق چرکی پدیدار می شوند و بوی تنفسی دام بدلیل حضور این ضایعات دهانی بد بو است. مشابه با این رخداد ترشحات سروزی بینی نیز چرکی می گردند . چنانکه بیماری پیشرفت می نماید کانون های نکروزه شونده مخاطی در حفره دهانی ظاهر می شوند ، این ضایعات نکروزه پراکنده (باقطر 1-5 میلیمتر) هستند ، ضایعات فوق در ابتدا سرسوزنی بوده ولی به سرعت بزرگ شده تا پلاک های خاکستری یا غشاهای کاذب زرد رنگی را ایجاد نمایند . ضایعات ابتداعاً در سطح داخلی لب پائینی و مجاورت لثه، بر روی مخاط محل به هم پیوستن گونه ها و سطح پائینی زبان پدیدارمی شود ، پس از مدتی ضایعات یاد شده تمامی بخش های زبان شامل پشت زبان را دربر می گیرد و در مواردی نیز چنان گسترده می شود که همه ضایعات باهم یکی می شوند . عموماً ضایعات فوق به رنگ خاکستری ، تاحدی برآمده و به وضوح نکروزه می باشند . بافت های نکروزه افتاده و ناحیه خام قرمزرنگی با لبه های مضرس برجای می گذارند و یک ناحیه تخریشی را پدید می آورد . در این بیماری هیچ نوع تاولی درهیچکدام از مراحل بیماری دیده نمی شود . در برخی موارد ضایعات پوستی در میان دوراه ، کیسه بیضه ، پهلو ، سطوح داخلی ران و گردن دیده می شود . پوست این نواحی مرطوب سرخ رنگ و نهایتاً پوشیده از دلمه می شود .
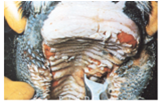
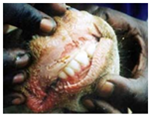
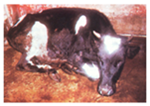
پس از یک دوره ناخوشی 3 تا 5 روزه دمای بدن بطور ناگهانی دچار افت شده و همراه با آن ضایعات دهانی بدتر گردیده ، تقلای تنفسی ، سرفه ، کم آبی شدید و گاهی درد های شکمی مشاهده می گردد . اسهال معمولاً بدنبال این کاهش تب (2 تا 3 روز پس از پیدایش ضایعات دهانی) ایجاد می شود . در شروع اسهال معمولاً فراوان و آبکی است اما در مراحل انتهائی ممکن است حاوی موکوس ، خون و بافت پوششی کنده شده باشد.درد های متعدد شکمی، زورپیچی و تشنگی غالباً به همراه اسهال وجود دارد و دام ممکن است در نتیجه کم آبی تلف شود . تقلای تنفسی [21] در مواردی ممکن است دیده شود و دانه ها یا جوش های مخاطی پردی [22] در نقاط کم پشت مو همچون زیر بغل ها و کشاله های ران بروز نماید . معمولاً 6 تا 12 روز پس از بروز علائم دام زمین گیر شده و دمای بدن به شدت کاهش می یابد و آنگاه در طی 24 ساعت دام تلف می شود . میزان تلفات بسته به نژاد ویروس متفاوت می باشد.در صورت بقای دام دوره نقاهت معمولاً طولانی بوده که عموماً توام با عفونت های ثانویه است . گاو های آبستن معمولاً در طی این دوره سقط می کنند .
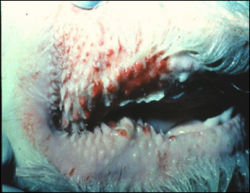

در مناطقی که بیماری بومی است مقاومت در برابر بیماری بالا بوده و اشکال تحت حاد و پوستی بیماری تظاهر می نماید . در شکل تحت حاد بیماری واکنش تب ملایم بوده و بی اشتهائی و رخوت توامان با تب مشهود نیست. التهاب مخاطات تنها حالت نزله ای داشته و هیچ نوع اسهال خونی دیده نمی شود . زخم هائی در شیردان بوجود آمده که بدون نشانه های بالینی است . در شکل غیر معمول بیماری تب نامنظم بوده ، اسهال بصورت خفیف ایجاد شده و یا اصلاً دیده نمی شود . در شکل پوستی بیماری واکنش های عمومی وجود نداشته و جوش های چرکدار(پوستول) کوچکی بر روی گردن و روی شانه ها ، سطح داخلی ران ها و روی کیسه بیضه ایجاد می شود .
ویروس مربوط به اعقاب نوع 2 می تواند در گاو تب کوتاه مدت ملایمی را پدید آورد که همراه آن پرخونی مختصری در غشاهای مخاطی بوجود می آید . نواحی کانونی برآمده ای از نکروز های پوششی بی رنگ را ممکن است در لثه پائینی و تعدادی پرد گونه ای سائیده شده در برخی از دام ها دید که این گونه ضایعات موقت هستند . ترشحات سروزی مختصری را می توان در چشم یا بینی یافت ، این ترشحات معمولاً مخاطی چرکی نمی شوند . اغلب دامهای آلوده بطور بارزی افسرده نیستند و بطور معمول به چرا و رفتار عادی ادامه می دهند . عفونت ناشی از ویروس طاعون گاوی اعقاب نوع 2 را به سختی می توان در گاو تشخیص داد ، ولی به هر حال این ویروس در صورت انتقال به گونه های وحشی چون گاومیش آسیائی، زرافه ، ایلند(نوعی آهوی درشت و گاو مانند) و کمتر در کودو(گوزن آفریقائی) موجب بیماری شدیدی می شود . در گاومیش عموماً بیماری طاعون گاوی مشابه گاو بوده اما بیماری های غدد لنفاوی[23] ، ضایعات پوستی شاخی شده شبیه پلاک و التهاب ملتحمه و قرنیه [24] شدید نیز ممکن است دیده شود .
نشانه های بالینی و ضایعات مشابهی نیز در گوسفند و بز ایجاد می شود اما به نظر نمی آید که بیماری از این گونه ها به سادگی به گاو منتقل گردد . خوک های اروپائی به بیماری حساس هستند ولی بیماری به لحاظ بالینی نامشهود و پنهان بوده و بصورت تحت بالینی است، در حالی که نژاد های آسیائی خوک ها بیماری با نشانه های معمول تظاهر کرده ، اشکال فوق حاد و حاد بیماری قابل مشاهده است و میزان تلفات بالا می باشد . انتشار بیماری از خوک به گاو معمول بوده و خوک ها را بعنوان یک منبع خطرناکی مطرح می سازد . در برخی مناطق بیماری طاعون گاوی بصورت پنومونی ظاهر می گردد و علائمی مشابه با پلوروپنومونی مسری نشان می دهد . نشانه های بالینی در طاعون نشخوارکنندگان کوچک خیلی شبیه با طاعون گاوی است . بز های مبتلا تب ، تخریش های مخاطی در دهان ، اسهال و پنومونی را نشان می دهند . گاهی تخریش هائی در فرج یا حشفه وجود داشته و در مواردی نیز سقط گزارش شده است .
تشخیص آزمایشگاهی:
به لحاظ وضعیت تابلوی خونی درطی یک عفونت طبیعی و یا پس از انجام مایه کوبی در گاو و گوسفندان و خوک هائی که بطور تجربی آلوده شده اند ولی نشانه بالینی ندارند یک لوکوپنی بارزی را می توان مشاهده نمود . شمارش کلی گویچه های سفید خون به کمتر از 4000 در هر میکرولیتر می رسد و در این میان چند روز بعد یک نوتروفیلی بطور آشکار پدیدار می گردد.
به لحاظ سرم شناسی آزمون ثبوت مکمل مناسب ترین و دسترس ترین آزمون تشخیصی است . میزان پادتن های ضد ویروسی موجود در سرم حدود 14 روز پس از شروع نشانه های بالینی به اوج خود می رسد . در دام بهبود یافته ای که مدت طولانی از آغاز بیماری در آن می گذرد سطح سرمی پادتن ها به اندازه ای نیست که بتوان با این آزمون آن را تشخیص داد ، در چنین شرایطی آزمون خنثی سازی سرمی (SN) بکار می رود . از دیگر شیوه های تشخصی سرمی می توان به تعیین پادتن درخشان ، و پراکسیداز ایمن اشاره نمود ، آزمون الیزا یک شیوه تشخیصی دقیق،قطعی و آسان بوده که می توان با آستفاده از آن طاعون گاوی را از طاعون نشخوا کنندگان کوچک تفکیک کرد و همچنین ارزیابی ایمنی نقطه ای [25] که یک آزمون سریع ومناسب برای گله است. آزمون های تشخیص سرمی معمولاً در مناطقی که بیماری ثابقه قبلی داشته بکار می روند ولی در شرایطی که بیماری برای اولین بار در یک حوزه اشاعه یافته بایستی اقدام به جداسازی ویروس و تشخیص نوع آن داد . آزمون های فوق می توانند به منظور پایش در یک منطقه بکار آیند ولی در تفکیک دام های واکسینه ناکارآمد هستند .
یک شیوه تشخیص دیگر انتقال تجربی بیماری است . این روش در صورت نبود امکانات جداسازی آسان و عدم حفاظت مناسب راه خطر ناک و پرهزینه ای است . در گروه گیرنده بایستی یک یا چند دام ایمن شده وجود داشته باشد . با تزریق داخل وریدی 5 میلی لیتر از خون دامی که در اوج بیماری است به گاو حساس نشانه های بالینی در طی 3-10 روز آشکار می گردد . در این شیوه از گوسفند نیز بعنوان یک گیرنده می توان استفاده کرد ولی تنها نشانه بیماری یک تب ملایم بوده و ممکن است که تخریش های دهانی آشکار نگردد .
یکی دیگر از فن آوریهای تشخیصی مناسب جهت تعین پادگن ویروسی بهره گیری از شگرد انتشارایمنی داخل آگار ژلاتینه (AGID) است . دراین روش نمونه های آزمایشی توسط سوزن از غدد لنفاوی بعنوان پادگن تکه برداری می شوند . بایستی توجه داشت که زمان نمونه برداری در این روش محدود می باشد که بایستی 3 تا 5 روز پس از شروع تب بدان مبادرت ورزید تا اینکه به درصد بالائی از تشخیص نائل شد . پس از شروع اسهال نسبت موارد مثبت آزمون به سرعت کاهش می یابد . اگر چه این روش بطور میدانی قابل اجرای است ولی باید توجه داشت که با استفاده از این آزمون نمی توان نومنه های مثبت طاعون گاوی را از طاعون نشخوارکنندگان کوچک تفکیک نمود. از دیگر شگرد های مناسب تشخیصی برای تعیین حضور پادگن ویروسی می توان به آزمون ترسیب آگار ژلاتینه و الکتروفورز مخالف ایمنی [26] اشاره کرد که در آن نمونه های موردآزمایش عبارتند از مدفوع، خراش برداری های مخاط دهانی ، ترشحات چشمی و بینی دامی که در مراحل اولیه بیماری است . امروزه جداسازی و تعین نوع ویروس با استفاده از فن آوری کشت بافتی کاملاً عملی است . در این شیوه نمونه های مورد استفاده غدد لنفاوی تازه بوده و زمان مناسب 3 تا 6 روز پس از شروع تب می باشد . یاخته های اجدادی لنفوبلاستوئید میمون مارموزت (B95a) از مناسب ترین محیط های کشت برای ویروس طاعون گاوی است .
تفکیک ژنوم ویروسی با استفاده از روش واکنش زنجیری پلیمری (PCR) و رونوشت برداری معکوس واکنش زنجیری پلیمری (RT-PCR) امکان پذیر است . با این روش ها می توان نوع اعقاب ویروسی(1و2و3) را تعین کرد و همچنین ویروس طاعون گاوی را از طاعون نشخوار کنندگان کوچک تفکیک نمود .
پیش از اقدام به نمونه برداری و ارسال آن بایستی سازمان مربوطه را از این اقدام مطلع ساخت . به منظور ممانعت از انتشار بیماری نمونه ها بایستی در تحت یک شرایط حفاظتی به آزمایشگاه های مرجع و تائید شده ارسال گردد .
ویرمی را می توان یک یا دو روز قبل از شروع تب مشاهده نمود . این ویرمی 1 تا 2 روز پس از افول تب نیز در خون قابل پیگیری است . نمونه های که به منظور جداسازی پادگن یا تعین RNA ویروس اخذ می شوند بایستی در مرحله اوج تب و بروز ضایعات دهانی و پیش از شروع اسهال نمونه گیری شوند ، در این مرحله تیتر ویروسی در بیشیه میزان خود است . خون حاوی هپارین یا EDTA نومنه ترجیحی جهت جداسازی ویروس در دام زنده است . درصورت ممکن بایستی نمونه های خونی را از چند حیوان تهیه نمود . همچنین می توان از سرم ، سوآپ های اشکی، بافت های نکروزه ضایعات دهانی وتکه برداری با مکش سوزنی از غدد لنفاوی سطحی بعنوان نمونه بهره گیری نمود . در هنگام کالبد گشائی نمونه ها را بایستی از طحال، غدد لنفاوی(پیش کتفی و مزانتریک) و لوزه ها برداشت نمود . ایدائل ترین ضایعات پس از مرگ دردام زمانی بدست می آید که دام فوق در طی مرحله تب معدوم شده باشد . انتخاب دوم دام محتضری است که معدوم گردیده . نمونه های مورد آزمایش RT-PCR را می توان از غدد لنفاوی ، لوزه ها و خون (لنفوسیت های خون محیطی) بدست آورد. طحال بدلیل محتوای خونی بالای آن مطلوبیت کمتری در نمونه گیری دارد . یک سری اضافه دیگری از نمونه های بافتی به منظور آسیب شناسی و ایمنی شناسی شیمی بافتی [27] بایستی جمع آوری گردند . علاوه بر بافت های دیگر، موارد ذیل نیز شامل آن میشوند: قاعده زبان، غدد لنفاوی پس حلقی و پلک سوم . نمونه های که جهت جداسازی ویروس اخذ شده اند بایستی در مجاورت یخ ولی یخ نزده ارسال گردند .
یافته های کالبد گشائی:
در شکل حاد بیماری لاشه دامی غالباً کم آب بوده و لاغری مفرط دارد، همچنین شواهدی دال بر اسهال و ترشحات مخاطی چرکی در بینی موجود است. چشم ها حالت به گود رفته دارند.اصلی ترین یافته های کالبد گشائی را در مجرای دستگاه گوارشی می توان یافت . بر روی مخاطات لوله گوارشی نواحی نکروزه ، پراکنده و کوچکی را می توان یافت . جدا شدن بافت های نکروزه در این مجرا بصورت تخریش های عمقی با بستری سرخ و دیواره هائی تیز تظاهر می کند که ممکن است با به هم پیوستن این نواحی تخریش های گسترده تری پدیدار گردد . این تخریش ها را می توان در دهان ، حلق، کام نرم و ثلث ابتدائی مری یافت ، همچنین ممکن است که ضایعات فوق بداخل حفرات بینی نیز نفوذ نمایند . ضایعات مشابهی نیز بر روی مخاط شیردانی دیده می شود، بطوری که بصورت قرمز(پرخونی شدید) ومتورم نمایان شده و خونریزی های زیر جلدی کوچک و متعددی را از خود نشان می دهد. این تغییرات را بیشتر در ناحیه باب المعدی[28] می توان دید. در پیش معده ها(هزارلا، نگاری ،شکمبه) هیچ گونه ضایعه ای مشاهده نمی شود ، البته در مواردی ممکن است که تنها بر روی پرد های شکمبه پلاک های نکروزه را یافت و همچنین در هزارلا تخریش ها و خونریزی هائی را مشاهده نمود. گاهی ممکن است که کانون نکروزه سفید رنگی در پلاک های پایر بوجود آید که در کنار این نواحی نکروز ، تخریش و حالت پوسته دادن مشهود است .در روده کوچک ضایعه ای دیده نمی شود . درمجرای روده بزگ ممکن است خون و لخته های خونی را دید، گاهی دیواره های روده بزرگ خصوصاً قولون بالائی آماسی بوده و تخریش و پرخونی در آن مشهود است . در حیواناتی که بطور حاد تلف شده اند دریچه ایلئوسکال ، لوزه های سکومی ، ستیغ های طولی چین های سکومی و مخاطات رکتومی و سکومی به مقدار زیادی پرخون هستند ، در موارد مزمن این قسمت ها تیره رنگ می شوند و ضایعه ای را بوجود می آورند که به خطوط ببری[29] یا خطوط گورخری[30] معروف است البته بایستی توجه داشت که در دیگر موارد اسهال نیز این نوع خطوط ببری پدیدار می شوند که ناشی از عمل زورپیچی در دام است . در مخاطات مهبلی و فرجی نیزممکن است پرخونی ، تورم و تخریش دیده شود . مشخصه آسیب شناختی بیماری طاعون گاوی عبارت است از تخریب گسترده لنفوسیتی که خصوصاً در غدد لنفاوی قابل توجه می باشد . غدد لنفاوی معمولاً متورم و آماسی هستند ، طحال ممکن است بدرجاتی از حد معمول خود بزرگ تر باشد ، در کیسه صفرا خونریزی های سرسوزنی(پتشی) و کشمشی(اکیموز) دیده می شود و گاهی آمفیزم،پرخونی و برنکوپنومونی ثانویه درریه ها مشهود است.
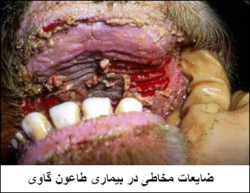
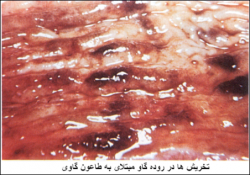
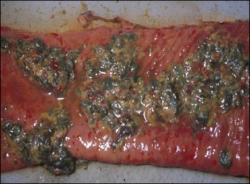
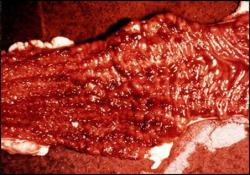
ضایعات در طاعون نشخوارکنندگان کوچک شامل تخریش های پوستی و مخاطی در ناحیه فرج و حشفه و مجرای گوارشی است . همچنین نشانه های پنومونی با یاخته های غول پیکرنیز قابل مشاهده است .
تشخیص تفریقی:
اصولاً زمانی می توان به بیماری طاعون گاوی مشکوک شد که تعدادی از دامهای گله با هم دچار تب ، تلفات و عفونت شده باشند و بیماری پدیدار شده با تخریش ها و التهاب های مخاطات گوارشی و اسهال مشخص گردد . همچنین تراوش بزاق ، افزایش ترشحات بیمی و اشک نیز از دیگر شاخص های این بیماری درگله هستند . تائید قطعی بیماری با انتقال بیماری به دام حساس یا آزمون های معتبر امکان پذیر است .
بیماری تب برفکی ٰ، تورم تاولی دهان و سپتی سمی هموراژیک از دیگر بیماری های همه گیر هستند که گله را درگیر نموده ولی به لحاظ تفاوت های بارز در امر تشخیص قابل تمیز هستند . انواع بیماریهای مخاطی شامل تب نزله ای بد فرجام(MCF) و بیماری مخاطی (BVD/MD) از موارد اشتباه برانگیز در امر تشخیص هستند . اما بایستی توجه داشت که در بیماری تب نزله ای بدفرجام موارد ابتلاء بطور انفرادی هستند و ندرتاً بصورت گروهی در گله پدیدار می شود و نهایتاً با کدورت قرنیه و نشانه های عصبی تفکیک می شوند . بیماری مخاطی همانند طاعون گاوی بصورت یک همه گیری در گله ظهور کرده ولی میزان تلفات در گله پائین است و یا ممکن است بصورت تگیر درگله ظاهر شده ولی چندان کشنده نیست . همچنین بیماری های دیگری چون سالمونلوز، نکروباسیلوز ، یون (پاراتوبرکولوز) ، تورم دهان پردی(پاپولی) گاوی و پلوروپنومونی مسری گاوی ممکن است درتشخیص ایجاد اشتباه نماید که باتوجه به جنبه های همه گیری ونشانه های مختص هرکدام تمیز بیماری امکان پذیر خواهد بود . در گوسفند وبزنیز بیماری زبان آبی و آبله گوسفندی وبزی ممکن است تشخیص را با اشتباه مواجه سازند .
جنبه های بهداشت عمومی:
هیچگونه گزارشی مبتنی بر ابتلای انسانی به بیماری وجود ندارد .
درمان بیماری:
اصولاً درمان موثری برای بیماری وجود ندارد واز طرفی به منظور جلوگیری از خطر انتشار بیماری بایستی از اقدام درمانی جهت حفظ دام بیمار اجتناب ورزید . انجام مایه کوبی در راستای درمان تاثیر معنی داری ندارد بطوری که اعمال آن درمرحله نهفته یا عفونی بیماری تا 48 ساعت پس از مایه کوبی هیچ گونه ایمنیتی فراهم نمی آورد .
کنترل و پیشگیری:
رئوس کلی اقدامات کنترلی درخصوص بیماری طاعون گاوی مبتنی بر سه راهکار است . اقدامات پیشگیرانه مبتنی بر کنترل آلودگی محیطی ؛ اقدامات پیشگیرانه مبتنی بر مایه کوبی ؛ اقدامات پیشگیرانه مبتنی بر پایش و مراقبت .
جهت کنترل آلودگی محیطی بایستی اقدامات زیر را انجام داد: حذف دامهای مبتلا و تحت تماس ، معدوم نمودن لاشه های دامی ، ضدعفونی کردن دامداری و حفاظت از مناطق عاری از آلودگی .توصیه FAO در خصوص کنترل آلودگی محیطی مبتنی بر تمیز کردن جایگاه دام ، وسایل دامداری لباس های کاراست که بعداً بایستی با ترکیبات اکسید کننده ای چون هیدرواکسید سدیم یا کربنات سدیم ضدعفونی شوند ؛ پیش از سوزاندن یا دفن کردن فضولات و فاضل آب بایستی به آنها کربنات سدیم افزوده شود. انجام پاستوریزاسیون یا جوشاندن شیر موجب غیرفعال شدن ویروس در شیر می گردد. پس از نجام ضد عفونی های لازمه دامداری بایستی تا 30 روز خالی مانده و بعد از این مدت اقدام به جدید دام نمود. زمانی که یک همه گیری در منطقه عاری از بیماری پدیدار می گردد بایستی حمل ونقل دام زنده و محصولات تازه دامی متوقف شود . تمامی دامهای حساس چه مبتلا و چه در معرض تماس بایستی کشتار شده و دردامداری مربوطه معدوم گردند . تمامی نشخوار کنندگان بایستی بعنوان دام حساس مورد توجه قرارگیرند و توجه خاصی نسبت به تمامی جانوران بومی[31](فون بومی) آن منطقه مبذول شود. وقتی که خطر بروز یک همه گیری وجود دارد یا زمانی که همه گیری گسترش است و احتمالاً از کنترل خارج خواهد شد بایستی مبادرت به مایه کوبی تمامی نشخوارکنندگان و خوک ها در منطقه تحت خطر نمود. این اقدام بایستی در خصوص نشخوارکنندگان وحشی که محتملاً حساس بوده و بعنوان حاملین بالقوه عفونت عمل می کنند نیزاعمال گردد. در مناطقی که بیماری بصورت بومی است اقدامات کنترلی عمدتاً مبتنی بر مایه کوبی با استفاده از واکسن های موثر است . در چنین مناطقی بایستی بصورت مرحله ای گله های حساس ، خصوصاً گاوهای یک ساله عموماً مایه کوبی شوند . وقتی در چنین مناطقی همه گیری پدیدار شد تمامی دامهای درگیر و تحت تماس مایه کوبی می شوند . نوع واکسن انتخابی بستگی به قابلیت دسترسی به گله ها جهت تکرار مایه کوبی دارد خصوصاً وقتی که از واکسن های تخفیف حدت یافته استفاده می گردد این امکان دسترسی از قدم های ضرور به شمار می رود . درصورتی که این دسترسی مقدور نباشد بکار گیری واکسن لاپینایز توصیه می گردد. در بحث ریشه کنی بیماری زمانی می توان به نتایج قابل توجهی رسید که اولاً با انجام مایه کوبی بتوان میزان وقوع بیماری تا سطح مناسبی کاهش داد و ثانیاً بتوان منابع آلودگی را حذف نمود، اساساً حیوانات وحشی آن مناطق بعنوان یک منبع بالقوه اشاعه بیماری هستند که در این راستا بایستی حذف گردند .
بزرگترین مشکل در برنامه مایه کوبی انتخاب واکسنی است که بدون داشتن عوارض جنبی و واکنش هاس شدید ایمنی بتواند یک ایمنیت درسطح قابل قبولی را در امهای مایه کوبی شده فراهم آورد . حساسیت به ویروس طاعون گاوی در گله های مختلف متفاوت بوده از این رو یک واکسن استاندادر ممکن است در گله ای ایجاد واکنش ایمنی کرده و درگله ای دیگر ایمنیت کافی را فراهم نسازد یا اینکه در گله ای ایمنیت بدهد ولی در گله ای دیگر واکنش شدیدی را در پی داشته باشد . از این رو واکسن ایدائل واکسنی است که درجات متنوعی از تخفیف حدت را داشته و برای گاو هائی با سطوح مختلفی از حساسیت ایمنیت قابل قبولی را فراهم آورد و ازطرفی نیز عوارض جانبی شدیدی را درپی نداشته باشد . مشکل دیگری که در اجرای برنامه های مایه کوبی مسئله ساز است فعال شدن ناخواسته عفونت های نهفته در حیوانات مایه کوبی شده می باشد خصوصاً وقتی که از واکسن هائس استفاده می گردد که به میزان کمتری تخفیف حدت یافته اند . دراین بازفعالی عفونت های نهفته بیشترین میزان مربوط به آلودگی های نهفته تک یاخته ها بوده اگرچه این امکان در مورد عفونت های باکتریائی و ویروسی نیز ممکن است. توصیه می گردد از مایه کوبی دامهائی که بصورت گسترده با انگل خارج گوشی رپیسفالوس آپندیکولاتوس درگیر می باشند ممانعت بعمل آید . مشکل بعدی در مورد مایه کوبی گوساله ها است . اگر این اطمینان وجود داشته باشد که گوساله ای از طریق آغوز پادتن بیماری طاعون گاوی را دریافت نکرده می توان در روز اول تولد این گوساله را تحت ماه کوبی قرار داد اما اگر این گوساله بواسطه آغوز دریافتی از مادرایمن شده ، دارای پادتن های مادر در سرم خود باشد تجویز واکسن قبل از 9 ماهگی در این گوساله ایمنی زا نخواهد بود .از طرفی این گوساله ها بسته به وضعیت ایمنی مادر دارای یک ایمنیت غیرفعالی[32] در طی یک دوره 4-8 ماهه خواهند بود . همواره بایستی به این نکته توجه داشت که حیوانات مایه کوبی شده ممکن است آلوده شده و بعنوان یک ناقل فعال عمل نمایند ازاین رو گوساله هائی که مایه کوبی شده یا بواسطه پادن های مادری ایمنیت نسبی دارند دصورت آلایش با ویروس از طریق راه داخل بینی قادر خواهند بود که ویروس بیماری را متعاقباً در محیط پخش نموده ودامهای در معرض تماس را آلوده سازند.
واکسن های بکار رفته بر علیه بیماری هم از نوع کشته و هم تخفیف حدت یافته هستند ولی نوع تخفیف حدت یافته آن که از محیط کشت بافتی بدست می آید بیشترین میزان ایمنیت زائی را دارد. در ایجاد این ایمنیت پروتئین های H و F موجود در پوشش خارجی ویروس ایفای نقش می نمایند. مایه کوبی دام برعلیه یک نوع نژاد ویروسی می تواند دام را درمقابل دیگر نژاد های ویروس حفاظت نماید. عمومی ترین نوع واکسن مصرفی از نژاد تخفیف حدت یافته ویروس طاعون گاوی است ، البته در برخی از کشورها از واکسن مخلوط طاعون گاوی و پلوروپنوموی مسری گاوان نیز استفاده می شود . ایمنیت بدست آمده از واکسن تخفیف حدت یافته حداقل تا 5 سال دوام داشته و به منظور دست یابی به بیشترین درصد دامهای ایمن شده در یک منطقه تجدید مایه کوبی بطور سالانه توصیه می گردد.
[1] negative sense
[2] transcription
[3] replication
[5] virion
[6] multimers
[7] leader RNA
[8] antigen-presenting cells
[9] signalling lymphocyte activation molecule
[10] casein kinase II
[11] Assembly
[12] Artiodactyla
[13] Kudu
[14] bushpig
[15] warthog
[16] wilde-beest
[17] Giant cell
[18] Focal necrotic stomatitis
[19] Gut-associated lymphoid tissues
[20] Signal transducers and activators of transcription
[21] Dyspnea
[22] maculopapular rash
[23] lymphadenopathy
[24] keratoconjunctivitis
[25] Dot-immunoassay
[26] Counterimmunoelectrophoresis
[27] immunohistochemistry
[28] Pyloric reginon
[29] tiger striping
[30] zebra striping’
[31] Native fauna
[32] Passive